QUESTÃO 1
(ENEM-2015)
O cobre presente nos fios elétricos e instrumentos musicais é
obtido a partir da ustulação do minério calcosita (Cu2S). Durante
esse processo, ocorre o aquecimento desse sulfeto na presença de
oxigênio, de forma que o cobre fique “livre” e o enxofre se
combine com o O2 produzindo SO2, conforme a equação química:
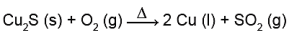
As massas molares dos elementos Cu e S são, respectivamente,
iguais a 63,5 g/mol e 32 g/mol.
(CANTO, E. L. Minerais, minérios, metais: de onde vêm?, para onde
vão? São Paulo: Moderna, 1996)
Considerando que se queira obter 16 mols do metal em uma reação
cujo rendimento é de 80%, a massa, em gramas, do minério
necessária para obtenção do cobre é igual a:
Resolução:
- Cu2S = 159g/mol
- Encontrando a massa de Cu2S em 80%
- 159g — 2 mols
- X — 16 mols
- X = 1272g
- 1272g — 80%
- Y — 100%
- Y = 1590g
QUESTÃO 3
(ENEM-2018)
O suco de repolho-roxo pode ser utilizado como indicador
ácido-base em diferentes soluções. Para isso, basta misturar um
pouco desse suco à solução desejada e comparar a coloração final
com a escala indicadora de pH, com valores de 1 a 14, mostrada a
seguir:

Utilizando-se o indicador ácido-base e a escola para determinar o
pH da saliva humana e o do suco gástrico, têm-se, respectivamente,
as cores:
Resolução:
Essa questão cobra um conhecimento sobre o valor do pH da saliva e do suco gástrico. A saliva saudável
tem o pH entre 6,8 e 7,2, ou seja, ela é quase neutra. O suco gástrico possui o ácido clorídrico, logo é
ácido e seu pH varia entre 1,5 e 2.
Portanto, tem-se:
I. Saliva: intervalo de pH entre 6,8 e 7,2, logo, fica dentro da cor roxa.
II. Suco gástrico: intervalo de pH entre 1,5 e 2, logo, fica dentro da cor vermelha.
QUESTÃO 6
(UNIUBE-MG)
Foi realizada uma festa de formatura do terceiro ano do ensino médio de uma escola de
Uberaba. Dois formandos estavam muito entusiasmados com a festa, que aconteceu em um dia quente de
primavera. Percebendo os fenômenos químicos e físicos que ocorriam ao seu redor, afirmaram:
I) O gelo, que está nos copos, após a ingestão dos sucos, está derretendo com muita facilidade
II) A carne do churrasco está ao ponto
III) Para acender o fogo na churrasqueira foi utilizado um pouco de etanol em gel, facilitando, assim, o
processo.
IV) A água da piscina não estava quente, porém visivelmente evaporava com facilidade devido à alta
temperatura ambiente.
Assinale a alternativa que contém a(s) afirmação(ções) em que há presença de um
fenômeno químico:
Resolução:
I- Fenômeno físico: ocorre apenas mudança de estado físico de sólido para líquido.
II- Fenômeno químico: Durante o cozimento da carne, as proteínas sofrem desnaturação, ou seja, perdem as
funções que desempenhavam anteriormente.
III- Fenômeno químico: o álcool em gel, ao sofrer combustão, é transformado em novas substâncias (no
caso,
gás carbônico e água).
IV- Fenômeno físico: ocorre apenas mudança de estado físico de líquido para vapor


